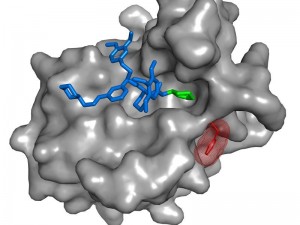
Der SAFit-Ligand (blau und grün) ist ein hoch selektiver Hemmstoff von FKBP51 (grau), einem Risikofaktor für stressbedingte psychiatrische Erkrankungen. Durch die Anlagerung von SAFit ändert sich die Ausrichtung einer Seitenkette des FKBP51 Proteins (rot). Dies ist bei dem sehr ähnlichen funktionalen Gegenspieler FKBP52 nicht möglich.
© MPI für Psychiatrie / Felix Hausch
Das FK506-bindende Protein 51 (FKBP51) ist ein Risikofaktor für psychische Erkrankungen, wie etwa Depressionen, die durch Stress ausgelöst werden. FKBP51 und sein Gegenspieler FKBP52 haben beide eine sehr ähnliche Struktur. Deshalb ist es schwierig Medikamente zu entwickeln, die nur FKBP51, nicht aber seinen Gegenspieler erkennen. Wissenschaftler haben jetzt den ersten wirkungsvollen und hoch selektiven Hemmstoff von FKBP51 entworfen. Der sogenannte SAFit-Ligand blockiert FKBP51 spezifisch. Dadurch wird das Wachstum von Nervenzellen in Zellkultur gefördert und bei Mäusen der Umgang mit Stress verbessert. Diese Forschungsergebnisse liefern strukturelle und funktionale Grundlagen für die Entwicklung neuer Antidepressiva.
FKBP51 und FKBP52 sind Proteine, die viele Vorgänge in unseren Zellen regulieren. Im Kontext psychischer Erkrankungen haben die beiden Proteine eine genau entgegengesetzte Wirkung auf Stresshormon-Rezeptoren im Gehirn. Während FKBP52 die Aktivität des Glukokortikoid-Rezeptors erhöht, hemmt FKBP51 diesen. Auf diese Weise spielen beide Proteine bei der Regulierung der Stressreaktion eine bedeutende Rolle.
Erstmals ist es Wissenschaftlern um Felix Hausch, Projektgruppenleiter am Max-Planck-Institut für Psychiatrie und Dozent an der Ludwig-Maximilians-Universität in München, nun gelungen, hochspezifische Hemmstoffe für FKBP51 zu entwickeln. „Ursprünglich haben wir einen chemisch-genetischen Ansatz verwendet und dann Schritt für Schritt die Bindung unserer Hemmstoffe verbessert“, erläutert Steffen Gaali, Post-Doc in der Projektgruppe von Felix Hausch. „Schließlich lagerte sich der wirksamste Ligand SAFit, ein selektiver Antagonist von FKBP51 durch induced fit, mehr als 10.000-mal besser an FKBP51 als an FKBP52 an.“ Der SAFit-Ligand passt nur deswegen in die Tasche von FKBP51, weil er dort die Seitenkette einer Aminosäure zur Seite schiebt. Diese Verschiebung ist bei FKBP52 nicht möglich.
Weiter untersuchten die Wissenschaftler Eigenschaften und Wirkung des SAFit-Liganden in Zellkultur und im Mausmodell. In Zellkulturen stimulierte SAFit die Ausbildung neuronaler Zelllinien. Im Gegensatz zu früheren FKBP51-Hemmstoffen zeigte SAFit bei Mäusen keinerlei Nebenwirkungen auf das Immunsystem. Darüber hinaus konnte SAFit depressionsähnliche Verhaltensweisen bei Mäusen lindern. Indem der SAFit-Ligand FKBP51 blockiert, wird dessen hemmende Wirkung auf den Glukokortikoid-Rezeptor im Gehirn abgeschwächt. Dadurch verbessert SAFit die Regulierung der HPA-Achse*, einem Schlüsselmechanismus bei der Stressbewältigung.
„Die Depression ist vermutlich eine biologisch nicht einheitliche Erkrankung und die wesentliche Schwierigkeit besteht darin, Antidepressiva auf die spezifischen zugrunde liegenden biologischen Veränderungen abzustimmen.“, erklärt Felix Hausch. „Patienten mit FKBP51-überaktivierenden Genvarianten oder mit einer hyperaktiven HPA-Achse können durch Genuntersuchungen für FKBP51 und/oder den Dex-CRF Test* klinisch identifiziert werden.“ Durch die Entwicklung des SAFit-Liganden zeigen die Wissenschaftler, dass sich selektive FKBP51 Hemmstoffe generell zur Behandlung stressbedingter psychischer Erkrankungen eignen.
* Die Hypothalamus-Nebennierenrinden-Achse (HPA-Achse, engl. hypothalamic–pituitary–adrenal axis) ist ein komplexes Wirkungsgefüge zwischen Hypothalamus, Hirnanhangsdrüse und Nebennieren. Die Wechselwirkungen zwischen diesen Organen sind bei der Kontrolle der Stressreaktion wichtig und regulieren viele Prozesse, einschließlich Verdauung, Immunsystem, Stimmungslage oder Emotionen. Die stressbedingte Abgabe des Corticotropin freisetzenden Faktors (CRF, engl. corticotropin-releasing factor) im Hypothalamus erhöht die Produktion von Cortisol in den Nebennieren. Cortisol selbst verursacht Anpassungen, wobei Alarmreaktionen einschließlich der Immunreaktion unterdrückt werden. Dadurch kann sich der Körper gegen den Stress wehren.
* Die Aktivität der HPA-Achse kann mit Hilfe des Dex-CRF Tests gemessen werden. Die Freisetzung von Cortisol ist in einigen Gruppen depressiver Patienten im Vergleich zu nicht-depressiven Kontrollpersonen deutlich erhöht, was auf eine Hyperaktivität der HPA-Achse schließen lässt.
Max-Planck-Gesellschaft, 1. Dezember 2014
Originalpublikation:
S. Gaali, A. Kirschner, S. Cuboni, J. Hartmann, C. Kozany, G. Balsevich, C. Namendorf, P. Fernandez-Vizarra, C. Sippel, A.S. Zannas, R. Draenert, E.B. Binder, O.F.X. Almeida, G. Rühter, M. Uhr, M.V. Schmidt, C. Touma, A. Bracher, F. Hausch. Selective inhibitors for the psychiatric risk factor FKBP51 enabled by an induced-fit mechanism. Nature Chemical Biology, 1. December 2014. doi:10.1038/nchembio.1699

