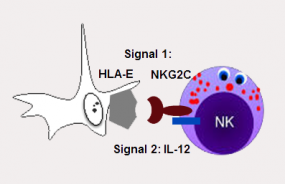
Killerzellen benötigen ein Doppelsignal um aktiviert zu werden. Signal 1 wird durch HLA-E auf den, mit den Viren infizierten Körperzellen vermittelt. Zusätzlich brauchen die Killerzellen eine Signal 2, das über IL2 und die Anwesenheit von Monocyten (nicht im Bild dargestellt) erfolgt. © dkfz.de
Wie Wissenschaftler jetzt herausfanden benötigen Killerzellen mindestens zwei Signale, um Zytomegalieviren bekämpfen zu können. Das Ergebnis könnte dazu beitragen, diese Vireninfektionen gezielter zu behandeln, die besonders für Leukämiepatienten nach einer Knochenmarkstransplantation gefährlich sind.
Eine Infektion mit humanen Zytomegalieviren verursacht bei gesunden Erwachsenen meist gar keine Symptome. Doch bei Personen mit einem geschwächtem Immunsystem, wie etwa Leukämiepatienten nach einer Knochenmarkstransplantation, kann das Virus zu lebensbedrohlichen Komplikationen führen. Auch für ungeborene Kinder sind Zytomegalieviren lebensgefährlich: Kein anderer Erreger wird während der Schwangerschaft so häufig von der Mutter auf den Fetus übertragen.
Eine gut funktionierende Körperabwehr kann die Viren normalerweise in Schach halten, in erster Linie über den „angeborenen Arm“ des Immunsystems*. Dessen wichtigste „Waffengattung“ sind die natürlichen Killerzellen. Ein kleiner Teil dieser Killerzellen trägt auf seiner Oberfläche das aktivierende Rezeptormolekül CD94/NKG2C. Genau diese Gruppe der Killerzellen vermehrt sich massiv bei einer Zytomegalievirus-Infektion. Die molekularen Signale, die dafür verantwortlich sind, waren bisher nicht bekannt und konnten nun entschlüsselt werden.
Das Forscherteam um Adelheid Cerwenka im Deutschen Krebsforschungszentrum wollte herausfinden, welche Faktoren für die, durch die Zytomegalieviren ausgelöste Vermehrung der Killerzellen nötig sind. Dazu kultivierte es mit Zytomegalieviren infizierte Bindegewebszellen zusammen mit Immunzellen aus dem Blut gesunder Spender.
Dabei stellte sich heraus, dass sich die Killerzellen nur dann vermehren können, wenn bestimmte andere Immunzellen – sogenannte Monozyten, die den Oberflächenmarker CD14 tragen – anwesend sind und den Botenstoffs IL-12 ausscheiden. Neutralisierten die Forscher das IL-12, so konnten sich die Killerzellen kaum noch vermehren. Aber für die Aktivierung der Killerzellen ist nicht nur der Botenstoff, sondern auch die Anwesenheit der Monozyten notwendig.
Außerdem vermehren sich die Killerzellen nur dann, wenn die mit dem Virus infizierten Zellen auf ihrer Oberfläche das Molekül HLA-E tragen. HLA-E ist der Bindungspartner des Rezeptors CD94/NKG2C auf den Killerzellen. Es ist nahe verwandt mit den Präsentationsmolekülen, die bei der erworbenen Immunität als „Präsentierteller“ für Antigene unerlässlich sind. Zellen die mit Zytomegalieviren infiziert sind produzieren vermehrt HLA-E.
Die Aktivierung der Killerzellen durch das Zytomegalievirus ist ein komplexer Vorgang, an dem viele verschiedene Moleküle beteiligt sind. Damit sich die Killerzellen vermehren müssen sie zwei verschiedene Signale erhalten: Signale 1 ist HLA-E vermittelt und Signal 2 erfolgt durch IL-12 und die anwesenden Monozyten.
„Diese Aktivierung erinnert stark an das „Doppelsignal“, das benötigt wird, um das erworbene Immunsystem scharf zu machen. Dessen T- und B-Zellen müssen nach dem aktivierenden Antigenkontakt (Signal 1) in der Gegenwart anderer, so genannter kostimulatorischer Signale (Signal 2) erst eine Vermehrungsphase durchlaufen, bis die Abwehr steht“, erklärt Adelheid Cerwenka. Sie fügt hinzu „Die genaue Kenntnis dieser Interaktionen kann in Zukunft helfen, Patienten mit lebensgefährlichen Zytomegalievirus-Infekten besser zu behandeln, indem wir die Aktivierung ihrer Killerzellen unterstützen. Da Killerzellen außerdem auch eine wichtige Rolle bei der Abwehr von Tumorzellen spielen, könnte das Ergebnis auch die Entwicklung von Krebs-Immuntherapien weiterbringen“.
*Die körpereigene Abwehr gliedert sich in das angeborene und das erworbene Immunsystem. Das angeborene System dient zur sofortigen Verteidigung des Körpers. Die Zellen des angeborenen Systems tragen keine spezifischen Rezeptoren, sondern reagieren gegen ein breites Spektrum von Keimen (verantwortlich dafür sind Fresszellen und Granulozyten) oder veränderten Körperzellen (hier liegt das Einsatzgebeit der Killerzellen). Im Gegensatz dazu tragen die T- und B-Lymphozyten, die zum erworbenen Immunsystem zählen, auf ihrer Oberfläche hochspezifische Rezeptormoleküle, die sich gegen Proteinkomponenten bestimmter Erreger richten. Die Ausreifung dieser Zellen ist ein komplexer Prozess, der einige Zeit in Anspruch nimmt. Deshalb vergehen einige Tage, bis die erworbene Abwehr einsatzfähig ist. Einige dieser Zellen leben nach einer erfolgreich bekämpften Infektion weiter und bilden das Gedächtnis des Immunsystems. Wenn sie später erneut auf den entsprechenden Erregern treffen, so müssen sie sich erst vermehren, bevor sie eine schlagkräftige Abwehr aufbauen können.
Deutsches Krebsforschungszentrum (DKFZ), 14.11.2014
Originalpublikation:
Alexander Rölle, Julia Pollmann, Eva-Maria Ewen, Anne Halenius, Hartmut Hengel und Adelheid Cerwenka: IL-12-producing monocytes and HLA-E control HCMV-driven NKG2C+ NK cell expansion. Journal of Cinical Investigation 2014, DOI: 10.1172/JCI77440

