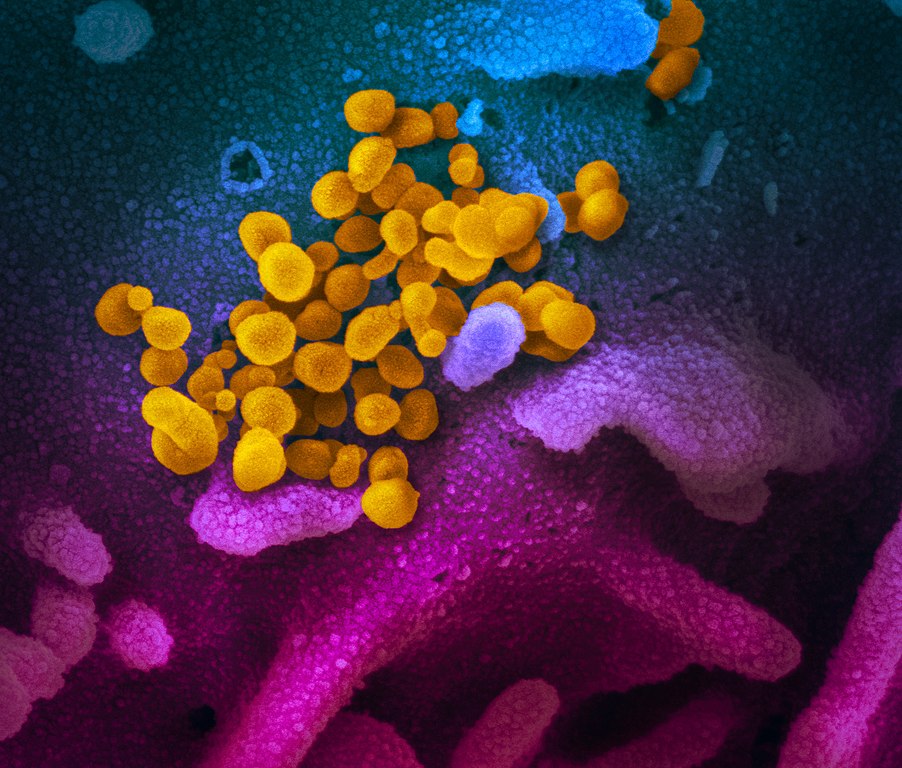
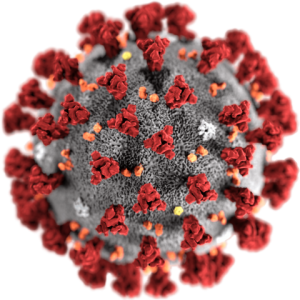
Impfstoffe sind eine der wichtigsten medizinischen Errungenschaften. Ihnen verdanken wir zu einem erheblichen Maße unsere hohe Lebenserwartung. So sind denn auch Impfstoffe die Hoffnungsträger im Kampf gegen die zur Zeit grassierende Corona-Pandemie. Die ersten vermutlich bald zugelassenen Impfstoffe basieren auf einer neuen Technologie: mRNA, die Bauanleitung für ein Protein. Sie haben den Vorteil, dass sie schnell und in großer Menge produzierten werden können. Aber auch den Nachteil, dass man mit ihnen beim Menschen keinerlei Erfahrung hat.

Eine der ersten größeren jungsteinzeitlichen Siedlung war Catal Höyük in Anatolien vor c.a. 9500 Jahren in der heutigen Türkei. Zur Blütezeit dieser Stadt wohnten dort rund 2000 Menschen dicht aufeinander gedrängt. Denn die Häuser standen Wand an Wand, so dass die Bewohner nur über die Dächer zu ihren Häusern gelangen konnten. Optimale Bedingungen für die Ausbreitung von Krankheitserregern. Dennoch wurde die Stadt 2000 Jahre lang bewohnt. Allerdings lebten dort damals noch keine Türken. Sie wanderten erst im 11/12. Jahrhundert aus Asien in dieses Gebiet ein. Die Bauern aus der Region von Catal Höyük wanderten später auch nach Europa und sind damit ein Teil unserer Vorfahren. © Wolfgang Sauber. CC BY-SA 4.0. Wikimedia Commons.
Seit der Mensch sesshaft geworden ist und sich in größeren Siedlungen niedergelassen hat, wird er immer wieder von Infektionskrankheiten heimgesucht. Da man sich dieses Phänomen früher nicht erklären konnte, machte man erzürnte Göttern dafür verantwortlich. Bereits in der Antike hatten sich die Menschen so stark vermehrt, dass Epidemien, wie etwa die Pest den Lauf der Geschichte beeinflussten. Raffte sie doch rund 30% der Bevölkerung dahin und machte die betroffenen Nationen so für Angriffe verwundbar. Der Pest verdankten vermutlich schon die Jamnaja ihre ungehinderte Wanderung, die sie vor rund 5000 Jahren aus der Steppe zwischen dem kaspischen und dem schwarzen Meer nach Europa führte. Wegen der Erkrankung, die sie auf ihrem Weg mitbrachten stießen sie kaum auf Widerstand der einheimischen Bevölkerung. Auch der Siegeszug der Muslime geht unter anderem auf das Konto der Justinianischen Pest, die am Ende der Antike über mehrere Jahrzehnte wütete. Nach einer mehrere Jahrhunderte währenden Pause suchte sie Europa erst wieder im 14. Jahrhundert unter dem Namen Schwarzer Tod heim. Doch auch die Pocken forderten früher viele Opfer. Auch ihr erlagen rund 30% der Erkrankten. In der Neuzeit wurde sie von der Tuberkulose abgelöst. Vor der Entwicklung eines Impfstoffes und der Pasteurisierung der Milch war sie so weit verbreitet, dass in Deutschland vermutlich jeder siebte an dieser Infektionserkrankung starb, die damals als Schwindsucht bezeichnet wurde. Daher waren auch viele berühmte Persönlichkeiten betroffen, wie etwa Schiller, Spinoza, Kafka,, Goethe, Chopin, Paganini, Boccherini, Dostojewski, Grieg, Orwell, Camus und Bebel. Die Tuberkulose hatte für die Gesellschaft so eine große Bedeutung, dass sich selbst die Künstler dieses Themas annahmen. So beschrieben etwa Giacomo Puccinis in La Bohème und Guiseppe Verdi in La Traviata die traurigen Folgen dieser Erkrankung. Und Thomas Mann verarbeitete das Leiden seiner eigenen Frau im Zauberberg. Eine andere Infektionskrankheit, die viele Opfer forderte, ist die Diphtherie.Die letzte Epidemie trat noch während des zweiten Weltkriegs auf, in deren Verlauf 3 Millionen Menschen erkrankten.

Edward Jenner impfte 1796 den achtjährigen James Phipps mit Kuhpocken, um ihn vor einer Infektion mit Pocken zu schützen. Welcome Images. CC BY 4.0. Wikimedia Commons.
Erst die Entwicklung von Impfstoffen und eine bessere Hygiene befreite die Menschheit von der immer wiederkehrenden Plage der Epidemien. In Europa leistete hierfür 1796 Edward Jenner Pionierarbeit, indem er einen Impfstoff gegen Pocken entwickelte. Später folgten Impfstoffe gegen Tollwut (1885), Typhus (1886), Cholera (1896), Pest (1897), Diphtherie (1923), Keuchhusten (1926), Tuberkulose (1927), Tetanus (1927), Grippe (1936), Kinderlähmung (1969), Mumps (1937), Masern (1968) und Röteln (1969), um nur einige der Krankheiten zu nennen, gegen die es inzwischen Impfstoffe gibt, denen wir in erheblichem Maße unsere heutige hohe Lebenserwartung verdanken.
Für eine Impfung kann man zum einen Totimpfstoffe verwenden, bei denen der Erreger in abgetöteter Form in den Muskel gespritzt wird. Beispiele hierfür sind Impfstoffe gegen Influenza, Cholera, Beulenpest, Hepatitis A oder Hepatitis B. Der Nachteil hierbei ist jedoch, dass die Reaktion des Immunsystems auf einen toten Krankheitskeim nicht so stark ausfällt und daher die Immunisierung meist nicht so lange anhält. Eine andere Möglichkeit ist ein sogenannter attenuierter Impfstoff, bei dem ein lebender Erreger verimpft wird, der jedoch durch das Heranzüchten auf nicht-menschlichen Zellen seine Virulenz verloren hat. Dies erreicht man etwa durch aufeinanderfolgende Kultivierung in artfremden Zellkulturen, embryonierten Hühnereiern oder Versuchstieren. Beispiele hierfür sind die Polio-Schluckimpfung (OPV), Bacillus Calmette-Guérin gegen Tuberkulose und manche Typhus-Impfstoffe. Der Nachteil dieser Impfungen besteht darin, dass der attenuierte Krankheitserreger in extrem seltenen Fällen mutieren kann und damit erneut krankheitserregend wird.
Normalerweise dauert die Entwicklung eines Impfstoffes gegen einen neuen Erreger rund zehn Jahre. Das liegt zum einen daran, dass die Attenuation für die Entwicklung eines Lebendimpfstoffen langwierig ist. Aber auch die Produktion von genügend Impfmaterial bei der Entwicklung eines Todimpfstoffes kostet viel Zeit. Oft kommen hierfür nur Teile des Erregers zum Einsatz, wie etwa das Hämagglutinin– und Neuraminidase-Protein des Influenza-Virus für den Grippe-Impfstoff. Bei einem neuen Impfstoff müssen die Sequenzen erst in entsprechende Vektoren kloniert werden, um sie dann für die Impfstoffherstellung vermehren zu können. Ist dann genügend Impfmaterial vorhanden müssen die verschiedenen Impfkandidaten zunächst im Tiermodell auf ihre Wirksamkeit und Unbedenklichkeit getestet werden. Erst danach können sie auch am Menschen erprobt werden. Das kann unter anderem deshalb länger dauern, weil es bei der Impfstofftestung bereits bei den vorklinischen Studien am Tier zu Rückschlägen kommen kann. Denn eine Impfung kann auch zur Bildung von eher unspezifischen Antikörpern führen. Dann wird etwa das Zielmolekül, das den Eintritt des Virus in die Zelle ermöglicht, nicht richtig blockiert. Solche Antikörper können eine Infektion verstärken. Man spricht dann von Infektionsverstärkenden Antikörpern. Dieses Phänomen beobachteten Forscher zum ersten Mal 1979 bei Rhesusaffen. Die Tiere hatten zunächst eine passive Immunisierung mit Antikörpern gegen das Dengue-Virus erhalten. Bei einer erneuten Infektion mit einem Virus eines anderen Subtyps litten die Tiere an einer verstärkten Infektion. Verschiedene Forscher berichten auch über den Nachweis von infektionsverstärkenden Antikörpern bei Coronaviren im Allgemeinen und COVID-19 im Besonderen. So führte etwa die Impfung von jungen Katzen mit dem Spike-Protein eines bei Katzen grassierendes Coronavirus zu einem früheren Tod der geimpften Tiere. Es bleibt abzuwarten, in wieweit sich diese Berichte für Covid-19 bestätigen.
Ein weiterer Effekt, den es im Tiermodell auszuschließen gilt, besteht in einer sogenannten molekularen Mimikry. Bei ihr ähnelt das Impfantigen in seiner räumlichen Struktur einem körpereigenen Protein. Mit diesem Trick versucht der Krankheitserreger sich vor einer Abwehrreaktion durch das Immunsystem zu schützen, so dass dieses die fremde Proteinstruktur nicht als solche erkennt. Diese Ähnlichkeit kann dazu führen, dass das Immunsystem eigene Proteine attackiert. Dann entstehen sogenannte Autoimmunerkrankungen. Auch bei einer Impfung kann diese Problem auftreten, wenn das Immunsystem Antikörper gegen ein Impfantigen bildet, das körpereigenen Proteinen ähnelt. Das war etwa bei dem Influenza-Impfstoff Pandemrix der Fall, der 2009/10 gegen die Schweinegrippe-Epidemie hergestellt wurde. Nachdem vor allem in skandinavischen Ländern auch viele Kinder und Jugendliche mit Pandemrix geimpft worden waren kam es zu einem vermehrten Auftreten von Narkolepsie gerade bei jungen Menschen. Bei dieser sehr seltenen Erkrankung fallen die Betroffenen immer wieder vorübergehenden in einen Sekundenschlaf. Bis 2015 wurden weltweit 1.300 Fälle der Krankheit mit Pandemrix in Verbindung gebracht. Eine geringe Zahl im Vergleich zu der Zahl der insgesamt geimpften Personen. Dennoch darf dies bei einem sicheren Impfstoff nicht passieren, was verdeutlicht, welche Herausforderung die Herstellung eines sicheren Impfstoffes darstellt. Bei einigen der von Narkolepsie Betroffenen konnten Antikörper gegen das für die Kontrolle des Schlaf-Wach-Rhythmus verantwortlichen Hormons Hypocretin nachgewiesen werden. Bei anderen Antikörper gegen seinen Rezeptor. Für den damaligen Konkurrenz-Impfstoff Focetria sind keine solchen Effekte bekannt. In Verdacht geriet der Impfverstärker von Pandemrix, AS03. Er könnte durch seine stark impfverstärkende Wirkung das Immunsystem dazu veranlasst haben, Antikörper gegen eigene Proteine zu bilden, was es normalerweise nicht tut. Ob er tatsächlich für die Nebenwirkung verantwortlich ist, konnte bisher jedoch nicht abschließend geklärt werden. Unter anderem auch deshalb, weil zur selben Zeit in Kanada ein Influenza-Inpfstoff eingesetzt wurde, der den gleichen Impfverstärker enthielt, aber offenbar nicht zu einer erhöhten Zahl an Narkolepsie-Fällen führte. Hinzu kommt, dass es auch während die Spanische Grippe grassierte zu einem vermehrten Auftreten von Narkolepsie kam. Es kann also auch sein, dass eine Influenza-Infektion bei sehr wenigen Menschen zu dieser Erkrankung führt.
Als 2002 in China das SARS-Corona-Virus grassierte versuchte man auch einen Impfstoff gegen das Virus zu entwickeln. Die verschiedenen Test-Impfstoffe bewirkten die Bildung von neutralisierenden Antikörpern. Doch als die Mäuse, Frettchen und Nicht-Humanen-Primaten dem Virus ausgesetzt wurden konnte sich dieser in den Tieren zwar nicht verbreiten. Aber er löste bei den geimpften Tieren eine Autoimmunreaktion in der Lunge aus, die durch die Aktivierung der zellulären Immunantwort gegen das Virus hervorgerufen wurde. Ähnliche Phänomene beobachtete man auch bei anderen Corona-Viren. Einige Forscher kamen zu dem Ergebnis, dass für diese Nebenwirkungen das Nukleocapsid (N)-Protein der Corona-Viren verantwortlich ist, eine Immunisierung gegen das Spike (S)-Protein dagegen unbedenklich sei. Versuche an Tieren, bei denen getestet wird, wie der Organismus nach einer Impfung reagiert, wenn er auf das Virus trifft, sind also bei der Entwicklung von Impfstoffen gegen Corona-Viren besonders wichtig. Bereits im April haben Forscher der chinesischen Firma Sinovac davon berichtet, dass eine Impfung mit Totimpfstoff von SARS-CoV-19 Rhesusaffen vor eine Infektion schützt. Allerdings muss man bei der Bewertung von Forschungsergebnissen chinesischer Pharmafirmen immer etwas vorsichtig sein. Denn das hierarchische und undemokratische System dort erlaubt es Forschern nicht, ihren Chef über Forschungsergebnisse zu informieren, die nicht mit seinen Erwartungen übereinstimmen. Doch auch die deutsche Firma BioNTech ließ bei den vorklinischen Tests für ihren mRNA-Impfstoffkandidaten BNT162b2 untersuchen, wie Rhesusaffen nach einer Impfung auf das Virus reagieren. Sie berichten, dass die Affen zumindest sechs bzw acht Tage nach der Virusinfektion gesund waren und ihr durch den Impfstoff trainiertes Immunsystem offenbar dazu in der Lage war das Virus an einer Vermehrung zu hindern. Allerdings betonen die Forscher auch, dass die Affen kein geeignetes Modell vor die COVID-19 Erkrankung darstellen, denn weder die geimpften noch die ungeimpften Tiere entwickelten die typischen Symptome einer Immunreaktion in der Lunge, wie wir sie vom Menschen kennen.
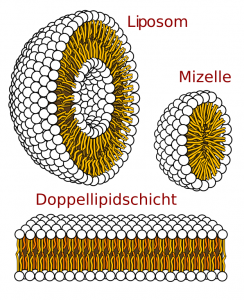
Einige der COVID-19-Impfstoffe basieren auf einer neuen Technologie, die bisher am Menschen noch nie ausprobiert wurde: mRNA. Diese Impfstoffe enthalten keine Virusproteine, sondern nur die Bauanleitung für ein Protein. In den meisten Fällen für das Protein, mit dessen Hilfe das Virus in die Zelle gelangt: das Spike Protein. Es bindet an das menschliche Protein ACE2 um in eine Zelle zu gelangen. Für den Impfstoff ist die mRNA von einem Liposom umgeben. Das soll die leicht abbaubare mRNA vor einem vorzeitigen Abbau schützen und ihr zudem das Eindringen in Körperzellen erleichtern. Denn, da die mRNA nur die Bauanleitung für die Produktion eines Proteins darstellt, muss sie in eine menschliche Zelle eindringen. Dort muss sie dem Proteinsynthese-Apparat zugeführt werden, der dann daraus das entsprechende Protein synthetisiert. Fragmente dieses Virusproteins werden dann von der Zelle über den sogenannten MHC-Komplex präsentiert, so wie auch alle anderen Protein, die eine Zelle produziert. Oder es wird in die Zellmembran eingebaut, da es ein entsprechendes Lokalisierungs-Signal enthält. Wenn nun die ständig im Körper patrouillierenden Immunzellen an einer Zelle vorbeikommen, die das Spike-Protein bildet, dann werden sie dieses als fremd erkennen, Alarm schlagen und eine Immunreaktion gegen Zellen auslösen, die dieses Protein bilden. oder die Bildung von Antikörpern veranlassen, die gegen das Protein gerichtet sind.
Der Vorteil einer Immunisierung mit mRNA besteht darin, dass man für eine wirksame Immunisierung nur relativ wenig mRNA braucht, im Vergleich zu den großen Antigenmengen, die man bei einer normalen Immunisierung mit Virusprotein benötigt. Und im Gegensatz zu einer Immunisierung mit einem DNA-Impfstoff verbleibt eine mRNA nur relativ kurz in der Zelle und wird nach einiger Zeit wieder abgebaut. Auch kann sie sich, anders als eine DNA nicht in das Genom der Wirtszelle integrieren. Bei Mäusen hat man mit dieser Technik bereits viel Erfahrung. Allerdings nur, um monoklonale Antikörper gegen ein gewünschtes Zielprotein zu gewinnen. Doch dazu wird die Maus nach einer zweiten Booster-Impfung geopfert, so dass man nicht weiß, wie gut die Tiere eine Impfung mit mRNA langfristig vertragen. In der Forschungsabteilung einer großen Pharmafirma bestellten wir immer dann monoklonale Antikörper von einem Hersteller, der diese durch mRNA-Impfung von Mäusen gewann, als wir mit normalen Impfmethoden keine Antikörper erhielten, weil das Impfantigen einem körpereigenen Protein der Maus zu ähnlich war. Es ist daher zu vermuten, dass mit der Methode der mRNA-Impfung Mechanismen des Immunsystems außer Kraft gesetzt werden, die eine Bildung von Antikörpern verhindern, die körpereigene Proteine erkennen. Doch wenn dies der Fall ist kann es zu Autoimmunerkrankungen kommen. Bisher hatten verschiedene Firmen vor allem daran gearbeitet eine mRNA-Impfung für die Krebstherapie zu entwickeln, da bei dieser schweren und nach wie vor meist immer noch unheilbaren Erkrankung die Hürden für neue Therapien relativ niedrig sind. Doch bisher ist auch auf diesem Gebiet kein mRNA-Impfstoff zugelassen. Selbst für die Immunisierung von Nutztieren gibt es bisher keinerlei Zulassung eines mRNA-Impfstoffes. Das sollte einem bei der Entscheidung für oder gegen eine mRNA-basierte Impfung gegen COVID-19 zu denken geben. Für die Impfstoffhersteller bietet die aktuelle Corona-Pandemie jedenfalls eine optimale Gelegenheit eine neue Technologie in kürzester Zeit zur Marktreife am Menschen zu führen, deren Entwicklung unter normalen Umständen vermutlich noch Jahre oder gar Jahrzehnte gedauert hätte.
Ein Nachteil der ersten Corona-Impfstoffe könnte jedoch darin liegen, dass sie über eine zu geringe Variabilität verfügen. Denn im Vergleich etwa zu den Influenzaimpfstoffen enthalten sie nur die Sequenz des Spike-Proteins einer einzigen Virusvariante. Bei den Influenzaimpfstoffen wählt man dagegen jedes Jahr neu eine Mischung von mindestens zwei verschiedenen Proteinen (Hämagglutinin– und Neuraminidase-Proteine) von drei verschiedenen Stämmen des Influenzavirus. Wenn nicht gleich mit einem attenuierten Virus geimpft wird, das heißt, mit dem gesamten, abgeschwächten Virus, gegen das das Immunsystem eine breite Palette an Immunreaktionen aktivieren kann. So stellt man sicher, dass dem Immunsystem über einen längeren Zeitraum trotz der hohen Mutationsrate des Virus immer noch passende Antikörper oder zytotoxische Immunzellen zur Verfügung stehen, um das Virus in Schach zu halten. Die Impferfolge der vergangenen Jahrzehnte beruhen vor allem auf Impfstoffen, bei denen mit attenuierten Erregern geimpft wurde. Inzwischen zeichnet sich immer mehr ab, dass auch das Corona-Virus eine höhere Mutationsrate zu haben scheint, als zunächst erwartet. Denn Virusvarianten aus England, Südafrika und Brasilien scheinen sowohl durch Antikörper von bereits von der Krankheit wieder genesenen, als auch von Seren geimpfter Personen schlechter erkannt zu werden. Dabei erwies sich etwa die Antikörperreaktion gegenüber der südafrikanischen Mutante B.1.351 um zwei Drittel schlechter im Vergleich zu der Spike-Variante, die im Impfstoff enthalten war. Wie sich die zelluläre Immunantwort gegenüber der südafrikanische Mutante verhält wurde nicht getestet. Im Extremfall könnte dies bedeuten, dass die bisher entwickelten Impfstoffe gegen diese Varianten nicht mehr richtig wirken.
Zweitinfektionen mit dem Virus scheinen bisher noch sehr selten zu sein. Eine Impfung mit einer Variante des Spike-Proteins, die nicht der aktuellen Form des grassierenden Virus entspricht könnte im Extremfall für den Geimpften einen echten Nachteil darstellen. Und zwar dann, wenn sein Immunsystem nach dem Prinzip der Antigenerbsünde auch gegen die neue Virusvariante immer nur die Antikörperversionen bildet, die es beim ersten Zusammentreffen mit dem Spike-Protein entwickelt hat. In diesem Fall könnten Personen, die eine Infektion des Virus durchgemacht haben gegenüber Geimpften im Vorteil sein, da ihr Immunsystem nicht nur Antikörper gegen das Spike-Protein hergestellt hat, sondern auch viele andere Antikörper, die gegen andere Proteine des Virus gerichtet sind. Diese Proteine mutieren normalerweise nicht alle gleichzeitig. Daher wird man die Impfstoffe wohl demnächst an die neuen Verhältnisse anpassen müssen, möglichst auch so, dass sie die Virusvariabilität so gut abdecken, wie dies die Influenzaimpfstoffe tun. Was allerdings eine gewisse Zeit dauern wird, da wir es bei Corona mit einem Virus zu tun haben, das wir noch nicht so gut kennen, wie etwa Influenza. Und weil die Entwicklung eines komplexeren Impfstoffes mehr Zeit in Anspruch nimmt.
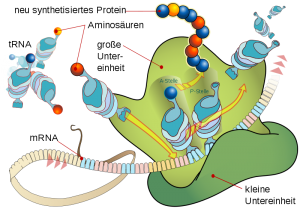
Die mRNA, die durch den Impfstoff in die Zelle gelangt wird von der Proteinsynthesemaschinerie genutzt um das entsprechende Protein herzustellen. © public domain. Wikimedia Commons.
Bei der Entscheidung für oder gegen eine Impfung muss man immer eine Kosten-Nutzen-Abwägung durchführen. Gerade für Risikogruppen kann es sinnvoll sein, das Risiko einer Impfung auf sich zu nehmen, selbst, wenn der Impfstoff noch nicht so ausgiebig getestet werden konnte, wie dies unter normalen Bedingungen der Fall gewesen wäre. Das gilt insbesondere für stark übergewichtige Menschen. Aber auch für solche mit Herz-Kreislauf Erkrankungen, bei denen der ACE2-Rezeptor als Eintrittspforte für das Virus eine wesentliche Rolle für den Krankheitsverlauf spielen könnte. Denn bei Menschen, die Bluthochdruck haben und Betablocker einnehmen ist die Zahl dieser Rezeptoren auf den Zellen erhöht, so dass in diese mehr Viren eindringe können. Aber auch für Menschen die unter Diabetes, Erkrankungen des Atmungssystems, der Leber, der Niere und Krebserkrankungen leiden oder die Raucher sind könnte sich eine Impfung lohnen. Generell nimmt das Risiko eines schweren Krankheitsverlaufes ab einem Alter von c.a. 55 Jahren mit jedem Lebensjahr kontinuierlich zu. Wobei man wissen sollte, dass zumindest die neuen mRNA-Impfstoffe möglicherweise stärkere Nebenwirkungen haben, als etwa eine Grippe-Impfung. Sie ähneln denen einer 12 Stunde dauernden Grippe. Am häufigsten sind, wie bei einer Grippe-Impfung, aber immer noch vorübergehende Kopfschmerzen (2%) und Abgeschlagenheit (3,8%). Nach der zweiten Booster-Impfung mit dem Impfstoff von Moderna litten einige Impfprobanden unter einer Schwellung am Arm, leichtem Fieber, Hitzewellen, Muskelschmerzen und Unwohlsein. Diese Symptome verschwanden jedoch nach 12 Stunden wieder. Sie könnten ein Indikator für eine gute Immunreaktion gegenüber dem Impfstoff sein. Im Vergleich zu einem schweren Verlauf einer COVID-19 Infektion sind sie jedoch immer noch vergleichsweise harmlos. Allerdings scheint der neue Impfstoff bei manchen Allergikern zu Nebenwirkungen zu führen. Menschen, die unter starken Allergien gegen Impfstoffe, Arzneimittel und Lebensmittel leiden, sollen sich daher lieber nicht impfen lassen. Inzwischen wird diskutiert, ob dieser Effekt auf einer Immunreaktion gegen das Polyethylenglycol (PEG) auf der Lipidhülle der Impfpartikel zurück geht. PEG ist in vielen Kosmetika und Pharmaprodukten enthalten. Weltweit haben inzwischen acht Personen nach der Impfung einen anaphylaktischen Schock erlitten (Stand 21. Dez 2020).
Für Menschen, die dagegen nicht zu einer Risikogruppe gehören mag es dagegen sinnvoll sein, erst einmal abzuwarten, als wie sicher und wirksam sich die Impfstoffe langfristig erweisen. Zu dieser Gruppe gehören besonders gesunde Kinder, Jugendliche und junge Erwachsene, denn ihr Immunsystem hat in der Regel keine Probleme damit, das Virus in Schach zu halten. Insbesondere da israelische und amerikanische Ärzte beobachtet haben, dass junge Männer im Alter zwischen 16 und 24 Jahren nach der Impfung eine Myokarditis, eine meist reversible Herzmuskelentzündung, entwickeln können. Laut dem israelischen Gesundheitsministerium sind davon zwischen einem von 3000 und einem von 6000 geimpften jungen Männern betroffen.
Quellen und weiterführende Informationen:
Should children get COVID vaccines? What the science says
Deaths from COVID ‘incredibly rare’ among children
Daten aus Israel: Impfung weniger effektiv seit Delta-Variante Dennoch schützt eine doppelte Impfung immer noch zu 93 Prozent vor einem schweren Verlauf, auch bei der Delta Variante.
Delta-Variante: Warum unter den Coronatoten immer mehr Geimpfte sind
COVID-19 vaccine side effects: The positives about feeling bad
Bericht von US-Experten: Herzprobleme nach Impfung möglich
Israel reports link between rare cases of heart inflammation and COVID-19 vaccination in young men
COVID vaccines and safety: what the research says
Fast-spreading COVID variant can elude immune responses
Neutralizing Activity of BNT162b2-Elicited Serum — Preliminary Report
COVID reinfections are unusual — but could still help the virus to spread
How to redesign COVID vaccines so they protect against variants
Original Antigenic Sin: How First Exposure Shapes Lifelong Anti–Influenza Virus Immune Responses
SARS-CoV-2: Allergische Reaktionen zu Beginn der Impfkampagne in Großbritannien
Suspicions grow that nanoparticles in Pfizer’s COVID-19 vaccine trigger rare allergic reactions
BioNTech-Impfstoff BNT162b2 erreicht Phase-III-Ziel: 95 Prozent Wirksamkeit
Grippeimpfung: Wie Pandemrix eine Narkolepsie auslöst
Pandemiepläne – Erkenntnisgewinn zwischen SARS und Schweinegrippe
Erste klinische Prüfung eines COVID-19-Impfstoffs in Deutschland genehmigt
Inaktivierter Virus-Impfstoff schützt im Tierversuch
Corona-Impfstoff von Biontech/Pfizer: Tierversuche ebneten den Weg
Fever, aches from Pfizer, Moderna jabs aren’t dangerous but may be intense for some
More people are getting COVID-19 twice, suggesting immunity wanes quickly in some