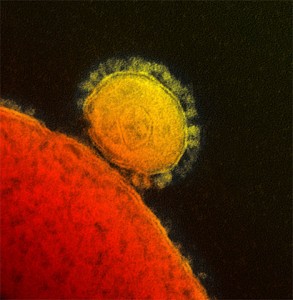
Im Kampf gegen das gefährliche MERS-Coronavirus (MERS-CoV) gibt es einen Hoffnungsschimmer: Möglicherweise reicht ein einziger Impfstoff aus, um alle momentan bekannten Virus-Varianten effektiv zu bekämpfen.
Infektionen mit dem MERS-Coronavirus (das Kürzel steht für „Middle East Respiratory Syndrome“) traten ursprünglich vor allem im Mittleren Osten auf. Bisher geht man davon aus, dass das Virus nur schwer von Mensch zu Mensch übertragen wird. Seine primären Wirtsorganismen sind vermutlich Fledermäuse, von denen es wahrscheinlich über Dromedare als Zwischenwirt sporadisch auf den Menschen übertragen wird. Erst vor kurzem sorgte eine Erkrankungswelle in Südkorea für Schlagzeilen.
Die zur Zeit zirkulierenden Erreger sind nicht identisch, sondern gehören zu verschiedenen genetischen Linien. Insgesamt kennt man bisher weltweit 23 verschiedene MERS-CoV-Varianten. Allein 20 von ihnen wurden im Rahmen der aktuellen Studie isoliert. Die Forscher der Uniklinik Bonn und des Deutschen Zentrums für Infektionsforschung (DZIF) haben nun drei Isolate der genetischen Hauptlinien genauer unter die Lupe genommen. Dazu versetzten sie die entsprechenden Viren mit Blutserum von Patienten, die eine MERS-Infektion überstanden hatten. Ergebnis: Die im Blut enthaltenen Antikörper waren in der Lage, jedes dieser Virus-Isolate effizient zu neutralisieren.
Gute Nachricht für Impfstoff-Entwickler
Demnach waren Patienten, die sich mit dem MERS-Erreger infiziert hatten, anschließend gegen alle drei ausgewählten Virus-Linien immun. „Das ist vor allem für die Entwickler von Impfstoffen eine gute Nachricht“, erklärt Doreen Muth. „Sie müssen nicht befürchten, dass ein von ihnen entwickeltes Vakzin nur gegen eine bestimmte Virus-Linie hilft.“
Auch in einem anderen Punkt ist die Studie für die Fachwelt von Interesse: Bislang war es nicht so einfach, MERS-Viren im Labor zu züchten. Die Vermehrung des Erregers erfolgt üblicherweise in Affenzellen, die in einer Nährlösung gehalten werden. Diese Zellen werden mit Patientenmaterial infiziert, um die Viren im Reagenzglas zu vermehren. Überraschenderweise erwiesen sich die Affenzellen aber als wenig effizient. Nur wenige Isolate konnten in ihnen angezüchtet werden. Deshalb versuchten es die Wissenschaftler darüber hinaus mit einer humanen Darmzelllinie. Dort war die Infektionsrate deutlich höher. Das ist eine wichtige Erkenntnis, denn Virologen sind für ihre Analysen auf eine effiziente Virusvermehrung angewiesen.
Das Team konnte zudem nachweisen, dass das Immunsystem nach einer Infektion Antikörper in die Atemwegs-Sekrete abgibt. Normalerweise sind die Nase und der Bronchialtrakt die Haupteinfallstore für das MERS-Virus. Die Antikörper sind dazu in der Lage diese Eintrittspforte effizient zu schützen.
Mangelhafte Krankenhaus-Hygiene verhalf dem Virus zur Ausbreitung
Allerdings kann sich dieser Schutz erst im Laufe einer Infektion oder nach einer Impfung herausbilden. Wenn das Virus den Körper unvorbereitet trifft, wird es dagegen höchst gefährlich: Seit seiner Entdeckung im Jahr 2012 haben sich über 1.100 Menschen mit dem Erreger infiziert. In 439 Fällen endete die Krankheit tödlich.
Experten gehen allerdings davon aus, dass viele Infektionen so leicht verlaufen, dass sie gar nicht bemerkt werden. Auch ist das Virus – im Gegensatz etwa zu SARS-Coronavirus – wohl nicht besonders infektiös. Damit es zu einer massenhaften Ansteckung kommt, müssen besondere Faktoren zusammen kommen. So sind die bisherigen Epidemien vermutlich unter anderem auf mangelhafte Krankenhaus-Hygiene zurückzuführen.
Rheinische Friedrich-Wilhelms-Universität Bonn, 10.07.2015
Originalpublikation:
Doreen Muth, Victor M. Corman, Benjamin Meyer, Abdullah Assiri, Malak Al-Masri, Mohamed Farah, Katja Steinhagen, Erik Lattwein, Jaffar A. Al-Tawfiq, Ali Albarrak, Marcel A. Müller, Christian Drosten, Ziad A. Memish; Infectious MERS-Coronavirus excretion and serotype variability based on live virus isolates from patients in Saudi Arabia; Journal of Clinical Microbiology; DOI: 10.1128/JCM.01368-15