ETH-Mikrobiologen um Markus Künzler haben ein bemerkenswertes Enzym in einem Pilz entdeckt. Sie möchten es nun nutzen, um damit neue Wirkstoffe zu entwickeln.
Ein Pilz voller Überraschungen: Der Dunkle Ölbaumtrichterling leuchtet in der Nacht und produziert für den Menschen interessante Peptide.© Noah Siegel, Wikimedia Commons, CC BY-SA 3.0.
Pilze scheinen ein schier unerschöpfliches Reservoir für neue Wirkstoffe zu sein. Ein solcher Fundus ist auch der Dunkle Ölbaumtrichterling (Omphalotus olearius), ein im Mittelmeergebiet häufig vorkommender Pilz, dessen Fruchtkörper in der Nacht fluoresziert.
Doch nicht dieser Special Effect macht ihn für die medizinische Forschung interessant, sondern ein Enzym in diesem Pilz, welches ETH-Forschende um den Mikrobiologen Markus Künzler jüngst entdeckten.
Dieses Enzym, OphA genannt, ist ein zentraler Bestandteil eines Stoffwechselweges zur Schädlingsabwehr des Dunklen Ölbaumtrichterlings. «Pilze wehren sich gegen Fressfeinde oder Konkurrenten mit einem Cocktail aus verschiedenen Giften – viele davon sind Proteine oder Peptide», sagt Künzler.
Der Dunkle Ölbaumtrichterling verwendet das Enzym OphA, um dem Rückgrat eines solchen Peptids mit zusätzlichen Methylgruppen zu versehen. Erst das auf diese Weise chemisch veränderte und nachträglich zu einem Ring geschlossene Peptid namens Omphalotin A wirkt als Gift. Der Pilz wehrt damit Schädlinge wie Fadenwürmer ab.
Schwer veränderbare Fertigungsstrasse
Peptide aus Pilzen dienen auch der Medizin als Wirkstoffe. Eines der bekanntesten ist Cyclosporin A. Dieses Peptid kommt seit bald 40 Jahren bei Organtransplantationen, Autoimmunkrankheiten und in der Krebsmedizin zum Einsatz.
Dieses Peptid ist ringförmig und trägt auf seinem Rückgrat dieselbe Art von Methylgruppen wie Omphalotin A. Die Ringform und die Methylgruppen sind dabei entscheidend für die vorteilhaften pharmakologischen Eigenschaften, insbesondere die orale Verfügbarkeit von Cyclosporin A. Letztere Eigenschaft ist nach wie vor eine grosse Hürde für peptidbasierte Medikamente.
Im Unterschied zu Omphalotin A, dessen Rückgrat, wie das der meisten Proteine und Peptide einer Zelle, durch das Ribosom hergestellt wird, wird Cyclosporin A durch ein riesiges, eigens dafür zuständiges Enzym aus den entsprechenden Aminosäuren zusammengebaut. Dieses Enzym funktioniert ähnlich wie eine Fertigungsstrasse in der Automobilindustrie. «Allerdings lässt sich diese Fertigungsstrasse biotechnologisch kaum verändern, um mit ihm Varianten von Cyclosporin A zu produzieren», sagt Künzler.
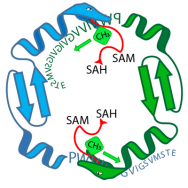
Das Enzym OphA (grüne und blaue Schlangen) bestückt das Vorläuferpeptid von Omphalotin A (Buchstabenfolge) mit Methylgruppen. In dieser Phase sind Enzym und Substrat fest verbunden. © Niels van der Velden und Mike Freeman / ETH Zürich
OphA ist nicht wählerisch
Mithilfe des Enzyms OphA könnte es jedoch möglich werden, nicht bloß Varianten von Omphalotin A, sondern weitere neuartige ringförmige Peptide herzustellen, die dank der eingeführten Methylgruppen ähnlich günstige pharmakologische Eigenschaften wie Cyclosporin A besitzen.
Grundlage dafür ist die Tatsache, dass die von OphA bearbeiteten Peptide von Ribosomen hergestellt werden und über eine Veränderung der entsprechenden Gene leicht zu verändern sind. Zudem scheint OphA in der Auswahl von Peptiden, die es chemisch verändern kann, nicht wählerisch zu sein. Das Enzym ist offensichtlich dazu in der Lage, Methylgruppen an eine große Bandbreite von verschiedenen Peptiden anzuhängen.
«Indem wir biotechnologisch unterschiedliche Ausgangspeptide herstellen und diese von OphA verändern lassen, können wir theoretisch völlig neue Peptide mit pharmakologisch interessanten Eigenschaften produzieren», erklärt Künzler.
So ließen sich mithilfe von OphA Bibliotheken von ringförmigen Peptiden mit Methylgruppen erzeugen, die als mögliche Wirkstoffe in Frage kommen. Solche Peptidbibliotheken könnten dann in einem weiteren Schritt nach Peptiden durchsucht werden, welche eine gewünschte biologische Eigenschaft, beispielsweise die Bindung an ein Zielprotein in der Krebstherapie, aufweisen.
Technologie zum Patent angemeldet
Die so identifizierten Peptide stellen vielversprechende Leitpeptide für die Entwicklung entsprechender Peptidtherapeutika dar, weil sie wegen der vorhandenen Methylgruppen mit hoher Wahrscheinlichkeit bereits günstige pharmakologische Eigenschaften aufweisen. «Dieser Ansatz bietet gegenüber Ansätzen, wo Methylgruppen chemisch erst im Nachhinein in die Peptide eingeführt werden, klare Vorteile sowohl bezüglich Kosteneffizienz als auch Erfolgswahrscheinlichkeit», sagt der Mikrobiologe.
Die Verwendung des Enzyms zum Einführen von Methylgruppen in Peptiden und das Verfahren zur Erzeugung entsprechender Peptidbibliotheken hat die ETH Zürich zum Patent angemeldet. Um den Nachweis zu erbringen, dass die Technologie funktioniert, hat Künzler einen KTI-Grant, vorerst noch ohne Industriepartner, eingeworben. Auch die Gründung eines Spin-offs steht zur Diskussion. «Zuerst müssen wir aber den ‚Proof-of-principle‘ erbringen, bevor wir für einen eventuellen Spin-off Finanzmittel einwerben können.» Die nächsten zwei Jahre seien dafür wohl entscheidend.
Begeisterte Fachwelt
Zumindest von der Fachwelt hat Künzler regen Zuspruch für seine Entwicklungen erhalten. An einer Konferenz über Peptide, die er kürzlich in Kanada besucht hat, sei das Interesse an seinem System gross gewesen. Einen Interessenten für den Erwerb einer Lizenz gebe es auch schon. «Es macht Spass, Grundlagenforschung in Richtung Anwendung zu begleiten», sagt er.
Das Naturstoffpotenzial von Pilzen schätzt Künzler grundsätzlich als sehr hoch ein. Weltweit gibt es mehrere Millionen verschiedene Pilzarten und die Zahl von vielversprechenden Naturstoffen ist dementsprechend gross. Er ist aber auch Realist und weiss, dass nur ein Bruchteil davon für Medikamente in Frage kommt – vielleicht werden es einige aus seiner Peptidsammlung schaffen.
von Peter Rüegg, ETH Zürich, 24. Juli 2017
Originalpublikation:
van der Velden NS, Kälin N, Helf MJ, Piel J, Freeman MF, Künzler M. Autocatalytic backbone N-methylation in a family of ribosomal peptide natural products. Nature Chemical Biology (2017). doi: 10.1038/nchembio.2393

