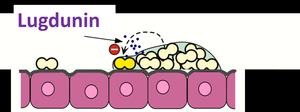
Schema zur Funktionsweise von „Lugdunin“: Auf den nasalen Epithelzellen (in Rosa) lebt natürlicherweise das Bakterium Staphylococcus lugdunensis (kleine weiße Doppelzellen), das den Infektionserreger Staphylococcus aureus (gelbe Doppelzellen) durch Bildung von „Lugdunin“ abtötet. © Andreas Peschel
In mancher Nasen unserer Mitmenschen lebt ein Bakterium, das weiß, wie man multiresistente Keime in Schach hält, wie Forscher nun herausgefunden haben. Dazu bildet Staphylococcus lugdunensis ein bisher unbekanntes Antibiotikum. Bei Versuchen an Mäusen bewies die „Lugdunin“ getaufte Substanz ihre Wirkung selbst gegen multiresistente Erreger, bei denen viele klassische Antibiotika versagen.
Weltweit gehören Infektionen mit Antibiotika-resistenten Bakterien, wie dem die Haut siedelnden Erreger Staphylococcus aureus (MRSA), zu den häufigsten Todesursachen. Der natürliche Lebensraum dieser Krankheitserreger ist in der Regel die menschliche Nasenhöhle. Forschern um Bernhard Krismer und Andreas Peschel an der Universität Tübingen war bei ihren Untersuchungen aufgefallen, dass Staphylococcus aureus immer dann selten auftrat, wenn sich das Bakterium Staphylococcus lugdunensis in einer Nase eingenistet hatte.
„Normalerweise werden Antibiotika nur von Bodenbakterien und Pilzen gebildet“, sagte Andreas Peschel. „Dass auch die menschliche Mikroflora eine Quelle für antimikrobielle Wirkstoffe sein kann, ist eine neue Erkenntnis.“ Als nächstes wollen die Forscher herausfinden, ob sich „Lugdunin“ tatsächlich therapeutisch nutzen lässt. So könnten etwa Risikopatienten mit den harmlosen „Lugdunin“-bildenden Bakterien besiedelt werden, um so das Risiko von MRSA-Infektionen zu senken. Eine genauere Analyse der Struktur von „Lugdunin“ ergab, dass es aus einer bisher unbekannten Ringstruktur von Aminosäurebausteinen besteht und damit zu einer neue Substanzklasse gehört.
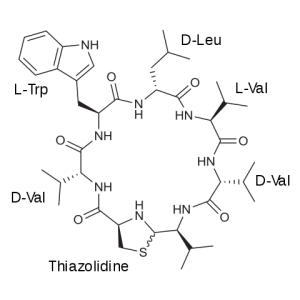
Struktur von Lugdunin. © Foreade. CC BY-SA 4.0. Wikimedia Commons.
Antibiotika-Resistenzen stellen Ärzte vor zunehmende Herausforderungen. „Es gibt Schätzungen, dass in den kommenden Jahrzehnten mehr Menschen durch resistente Keime als an Krebs sterben werden“, sagte Bernhard Krismer. Eine der Ursachen liegt dabei in der unsachgemäßen, oft unnötigen Nutzung von Antibiotika, wie etwa dem prophylaktischen Einsatz bei einem Schnupfen oder einer Grippe. Beide Infektionskrankheiten werden durch Viren verursacht, gegen die Antibiotika keinerlei Wirkung haben. Auch der bis 2006 weit verbreitete Einsatz von Antibiotika in der Tiermast als sogenannte Leistungsförderer sorgte für eine massive Zunahme an Resistenzbildungen.
Da viele der Erreger Teil unserer Mikroflora auf unserer Haut und unseren Schleimhäuten sind, können wir ihnen nicht aus dem Weg gehen. Besonders hoch ist das Risiko für Patienten mit ernsten Grunderkrankungen und einem geschwächten Immunsystem. Bei ihnen haben die Erreger leichtes Spiel. Die Forscher hoffen, das ihre Ergebnisse zur dabei helfen, nachhaltige Strategien zur Infektionsvermeidung zu entwickeln und neuartige Antibiotika aufzuspüren – auch und gerade im menschlichen Körper.
Universität Tübingen, 16 Juli 2016
Originalpublikation:
Alexander Zipperer, Martin C. Konnerth, Claudia Laux, Anne Berscheid, Daniela Janek, Christopher Weidenmaier, Marc Burian, Nadine A. Schilling, Christoph Slavetinsky, Matthias Marschal, Matthias Willmann, Hubert Kalbacher, Birgit Schittek, Heike Brötz-Oesterhelt, Stephanie Grond, Andreas Peschel & Bernhard Krismer: Human commensals producing a novel antibiotic impair pathogen colonization. Nature, 27. Juli 2016. doi: 10.1038/nature18634

