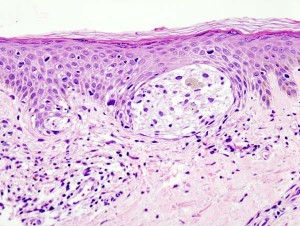
Gewebeschnitt durch ein Malignes Melanom. © KGH. CC BY-SA 3.0.
Mit Hilfe moderner Immuntherapien können mitunter sogar noch fortgeschrittene Tumoren erfolgreich behandelt werden. Doch wie kommt es, dass diese Medikamente nur bei manchen Patienten wirken und bei anderen nicht? Dieser Frage ist nun ein internationales Forscherteam nachgegangen. Im Mittelpunkt seiner Untersuchungen stand der Wirkstoff Ipilimumab, der bereits erfolgreich gegen schwarzen Hautkrebs eingesetzt wird.
Jedes Jahr erkranken rund 20.000 Menschen am schwarzen Hautkrebs, Tendenz weiter steigend. Schätzungsweise 3.500 dieser Patienten sterben jährlich an der Erkrankung, die jede Altersgruppe betreffen kann. Seit 2011 werden in Deutschland Patienten mit fortgeschrittenem schwarzen Hautkrebs mit dem monoklonalen Antikörper Ipilimumab behandelt, der gegen CTLA-4 gerichtet ist. Ipilimumab ist der erste zugelassene Wirkstoff aus der Klasse der so genannten Checkpoint-Inhibitoren. Bildlich gesprochen lösen Checkpoint-Inhibitoren die Bremsen des Immunsystems, so dass die Abwehrzellen sich wirkungsvoll gegen Tumoren richten können. Bei rund 20 Prozent der Patienten kann der Krebs mit dem Medikament über mehrere Jahre unter Kontrolle gehalten werden. Aber warum der Wirkstoff einigen Patienten hilft, anderen dagegen nicht, war bislang unklar.
Dieser Frage ist ein internationales Wissenschaftler nun nachgegangen. Bei der Untersuchung von 110 Patienten entdeckten sie einen interessanten Zusammenhang: Je mehr Mutationen der Tumor aufwies, desto wirksamer war das Medikament. Aber mit der Wirksamkeit von Ipilimumab geht auch eine verstärkte Produktion bestimmter Proteine, wie Granzyme A und Perforin einher, die das menschliche Immunsystem zur Zerstörung von Tumorzellen bildet.
„Unsere Beobachtungen lassen bislang aber noch keine präzisen Vorhersagen zu, wie ein Patient auf den Wirkstoff ansprechen wird“, erläutert Bastian Schilling, einer der Autoren der Studie. Die neuen Erkenntnisse zeigen aber, dass sich dahinter komplexe Mechanismen mit vielen Faktoren verbergen müssen. „Deshalb wollen wir im nächsten Schritt weitere Patienten untersuchen, um die genauen Wirkmechanismen zu entschlüsseln. So können wir die Immuntherapie in Zukunft hoffentlich noch individueller zuschneiden“, ergänzt Dirk Schadendorf.
Da die natürliche Funktion von Checkpoint Inhibitoren darin liegt, die Immunreaktion abzuschwächen ist damit zu rechnen, dass ein dauerhaftes Ausschalten dieser Immunbremse zu einer Überreaktion des Immunsystems und damit zu Autoimmunerkrankungen führen wird. Im Falle eines bösartigen Tumors muss man diese potentielle Nebenwirkung aber wohl als geringeres Übel in Kauf nehmen (Anmerkung der Redaktion von Scimondo).
Deutsches Krebsforschungszentrum (DKFZ), 11.09.2015
Originalpublikation:
Eliezer M. Van Allen, Diana Miao, Bastian Schilling, Sachet A. Shukla, Christian Blank, Lisa Zimmer, Antje Sucker, Uwe Hillen, Marnix H. Geukes Foppen, Simone M. Goldinger, Jochen Utikal, Jessica C. Hassel, Benjamin Weide, Katharina C. Kaehler, Carmen Loquai, Peter Mohr, Ralf Gutzmer, Reinhard Dummer, Stacey Gabriel, Catherine J. Wu, Dirk Schadendorf, and Levi A. Garraway: Genomic correlates of response to CTLA4 blockade in metastatic melanoma. Science 2015, DOI:10.1126/science.aad0095

