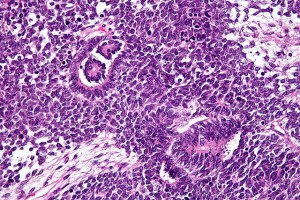
Wilms-Tumor (Nephroblastom). © Nephron. CC BY-SA 3.0.
Für kindliche Nierentumoren haben Wissenschaftler nun eine Reihe bisher unbekannter genetischer Ursachen identifiziert. Unter anderem bremst das Fehlen von microRNAs die Reifung der Nieren-Vorläuferzellen.
Wilms-Tumoren, auch als Nephroblastome bezeichnet, gehören zu den häufigen soliden Tumoren im Kindesalter. Sie treten meist vor dem sechsten Lebensjahr auf und zählen zu den sogenannten embryonalen Tumoren. Das sind Tumoren, die während der Organentwicklung durch eine fehlgeleitete Differenzierung von Geweben entstehen. Wilms-Tumore bilden sich aus Vorläuferzellen der Nieren des Embryos, die offenbar nicht korrekt ausgereift sind. Im Tumor findet man daher oft unterschiedliche Gewebestrukturen. Deshalb bezeichnete sie ihr Namensgeber Max Wilms 1899 auch als „Mischgeschwülsten der Niere“.
Bei der Suche nach den molekularen Ursachen von Wilms-Tumoren, besonders von deren Hochrisiko-Varianten, ist ein internationales Forscherteam nun fündig geworden. An den Forschungsarbeiten waren unter anderem das Team um Manfred Gessler am Biozentrum der Universität Würzburg und die Arbeitsgruppen von Marcel Kool und Stefan Pfister am Deutschen Krebsforschungszentrum in Heidelberg beteiligt.
Ausbremsen der Bildung von microRNAs verhindert Differenzierung
„Bislang waren drei Gene als mögliche Auslöser von Wilms-Tumoren bekannt. Wir konnten jetzt eine ganze Reihe weiterer Ursachen identifizieren“, erklärt Manfred Gessler. Da sind zum einen die Gene DROSHA und DGCR8. Sind diese defekt, kommt es unter anderem zu einer teilweisen Inaktivierung der molekularen Maschinerie, die für die Bildung sogenannter microRNAs verantwortlich ist. MicroRNAs wiederum können die Funktion einer Vielzahl von Boten-RNA-Molekülen regulieren und somit Zellen komplett umprogrammieren.
„Von embryonalen Stammzellen weiß man bereits, dass diese ohne microRNAs nicht in der Lage sind, sich in Zellen verschiedener Gewebe umzuwandeln“, sagt Gessler. Genau dies scheint auch bei Wilms-Tumoren der Fall zu sein: Sie entstehen, weil es einzelnen Vorläuferzellen der Nieren nicht gelingt komplett auszureifen. Deshalb verharren sie stattdessen in einem embryonalen Zustand, in dem sie sich schnell teilen müssen, um die Niere wachsen zu lassen.
Zwei Transkriptionsfaktoren betroffen
Neben den microRNAs fanden die Forscher aber auch Defekte in zwei Transkriptionsfaktoren. Die als SIX1 und SIX2 bezeichneten Proteine steuern die Aktivität anderer Gene. Von Tiermodellen war bereits bekannt, dass sie für die Bildung der Nieren unerlässlich sind. Darüber hinaus sind diese beiden Transkriptionsfaktoren in Wilms-Tumoren besonders aktiv. „Unsere Ergebnisse zeigen nun erstmals, dass die beiden Gene für diese Transkriptionsfaktoren in Wilms-Tumoren durch Mutationen verändert sind und dadurch auch in diesem Fall die Zellen in einem embryonalen Wachstumsmodus verharren“, erklärt Gessler.
Bekanntes Tumorgen weckt Hoffnung auf Therapie
Aber auch Tumorgene, die als Auslöser anderer Krebsarten bekannt sind, können zu Wilms-Tumoren führen. So konnten die Wissenschaftler zeigen, dass ein bestimmtes Gen, das an der Entwicklung von Neuroblastomen beteiligt ist – auch in Wilms-Tumoren aktiviert ist. „Das gibt Anlass zur Hoffnung, dass Therapien, die bei einem Neuroblastom erfolgreich sind, auch gegen Wilms-Tumoren wirksam sein könnten“, sagt Gessler.
Alt bekanntes Tumorsuppressorgen
Weiterhin zeigte ein Teil der Wilms-Tumoren eine Inaktivierung des bekannten Tumorsuppressor-Gens TP53. Eine Mutation in diesem Gen kann dramatische Genomveränderungen zur Folge haben, die bis zu einem Zerbrechen eines Chromosoms und einem Verlust oder einer Vermehrung von Chromosomenbruchstücken führen kann. Die Prognose von Tumoren mit solchen genetischen Veränderungen ist besonders ungünstig.
Personalisierte Therapie möglich
Die neuen Erkenntnisse können dazu beitragen, die Therapie zu verbessern. Derzeit überleben rund 90 Prozent der erkrankten Kinder, wenn sie eine Kombination aus Chemotherapie, Operation und anschließend einer erneuten Chemotherapie erhalten. Ein wesentlicher Faktor für das Gelingen einer Therapie besteht darin, Patienten mit sogenannten Hochrisiko-Tumoren rechtzeitig zu erkennen und entsprechend intensiver zu behandeln als solche mit einem geringen Rückfallrisiko. So sollen es künftig möglich sein die Belastungen und Folgeschäden für die Kinder möglichst niedrig zu halten.
Die heute routinemäßig eingesetzte feingewebliche Untersuchung und der klinische Befund liefern dafür zwar bereits wichtige Hinweise, reichen aber noch nicht aus. „Durch die Aufklärung der molekularen Ursachen besteht die Hoffnung, die Klassifikation der Tumoren zu verbessern, und im Rahmen einer personalisierten Medizin auch vermehrt zielgerichtete Therapien einsetzen zu können“, sagt Manfred Gessler.
Allerdings ist bisher noch nicht für alle neu entdeckten, genetischen Veränderungen bekannt, wie sie zur Tumorentstehung beitragen. Durch weitere Untersuchungen müssen nun die Kandidaten identifiziert werden, die am besten dazu geeignet sind, den Verlauf der Erkrankung vorherzusagen. Daher wird es auch noch eine Weile dauern, bis die neuen Erkenntnisse in neuen maßgeschneiderte Therapien umgesetzt werden können.
Deutsches Krebsforschungszentrum (DKFZ), 10.02.2015
Originalpublikation:
Mutations in the SIX1/2 Pathway and the DROSHA/DGCR8 miRNA Microprocessor Complex Underlie High-Risk Blastemal Type Wilms Tumors. Jenny Wegert, Naveed Ishaque, Romina Vardapour, Christina Geörg, Zuguang Gu, Matthias Bieg, Barbara Ziegler, Sabrina Bausenwein, Nasenien Nourkami, Nicole Ludwig, Andreas Keller, Clemens Grimm, Susanne Kneitz, Richard D. Williams, Tas Chagtai, Kathy Pritchard-Jones, Peter van Sluis, Richard Volckmann, Jan Koster, Rogier Versteeg, Tomas Acha, Maureen J. O’Sullivan, Peter Karl Bode, Felix Niggli, Godelieve A. Tytgat, Harm van Tinteren, Marry M. van den Heuvel-Eibrink, Eckart Meese, Christian Vokuhl, Ivo Leuschner, Norbert Graf, Roland Eils, Stefan M. Pfister, Marcel Kool, Manfred Gessler. Cancer Cell 2015, DOI: 10.1016/j.ccell.2015.01.002

