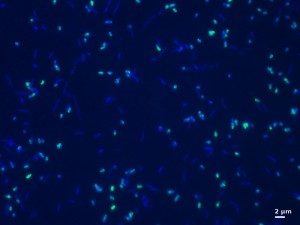
Angereicherte Kultur aus dem Reaktor unter dem Fluoreszenz-Mikroskop. Die grün angefärbten Zellen sind denitrifizierende Bakterien innerhalb ihrer bakteriellen Gemeinschaft.
© MPI für marine Mikrobiologie/ Theresa Hargesheimer
Neue Science-Studie könnte helfen, den Einsatz von Düngemittel effizienter zu gestalten und den Eintrag von Treibhausgasen zu reduzieren.
Der Einfluss der menschlichen Zivilisation auf den globalen Kohlenstoffkreislauf und die möglichen Folgen wie Klimawandel und globale Erwärmung sind lange bekannt. Daneben gibt es andere wichtige Prozesse, die weniger Beachtung finden. Es sind die massiven Einträge von Stickstoffverbindungen durch den Menschen. Jetzt hat ein Team von Wissenschaftlern die Parameter identifiziert, die darüber entscheiden, ob diese Stickstoffverbindungen bioverfügbar bleiben oder sie als inaktives Stickstoffgas in die Atmosphäre entweichen.
Luftstickstoff in Düngemittel umwandeln kann man erst seit Anfang des 20. Jahrhunderts mithilfe des Haber-Bosch-Verfahrens. Davor entstanden diese Düngemittel, also bioverfügbare Stickstoffverbindungen, nur auf natürlichem Wege. Stickstoff-fixierende Bakterien bilden Ammonium aus Luftstickstoff. Eine weitere Quelle sind Gewitterblitze, die dabei freigesetzte Energie lässt Stickoxide entstehen. Einen Teil dieser bioverfügbaren Stickstoffverbindungen wandeln denitrifizierende Bakterien wieder zu Luftstickstoff um.
Die globale Bilanz der Stickstoffverbindungen hat sich jedoch in den letzten Jahrzehnten entscheidend verändert. Jetzt kommt der Großteil nicht mehr aus natürlichen, sondern aus menschlichen Quellen. Die Folgen des massiven Einsatzes von Stickstoffverbindungen in Landwirtschaft und Aquakultur sind Eutrophierung von Seen, Süßwasserreservoirs und den Ozeanen. Auf lange Sicht wird auch die Atmosphäre beeinflusst.
Wie Kohlenstoff wird Stickstoff durch komplexe mikrobielle Prozesse umgesetzt. Mikroorganismen können bioverfügbares Nitrat auf zwei Wegen umwandeln. Entweder geht es über die Denitrifikation mit dem Endprodukt Stickstoffgas N2, das in die Atmosphäre entweicht und nun nicht mehr bioverfügbar ist. Als Nebenprodukt entsteht das Treibhausgas Stickoxid. Oder es geht über die Ammonifikation mit dem Endprodukt Ammonium. Das Ammonium bleibt bioverfügbar für Pflanzen, Getreide und andere Organismen.
Welcher Weg wird eingeschlagen?
Das Team um Marc Strous und Kollegen nahm Proben aus dem Wattenmeer vor Spiekeroog, die sie dann über einen längeren Zeitraum im Labor inkubierten, um gezielt den Einfluss verschiedener Umweltbedingungen zu untersuchen. Mit speziellen Methoden konnten sie den Weg des Stickstoffs verfolgen und bestimmen, welche mikrobielle Spezies zum Zuge kam. In 15 Experimenten gelang es ihnen, die drei Faktoren herauszuarbeiten. „Es sind das Verhältnis von Nitrit zu Nitrat, das Verhältnis von Kohlenstoff zu Stickstoff und die Wachstumsrate der Mikroorganismen,“ erklärte Beate Kraft, Erstautorin der Studie.
Marc Strous und sein Team vom Max-Planck-Institut für marine Mikrobiologie in Bremen setzten dabei moderne Genom-Analyseverfahren ein. Die Proben aus dem Wattenmeer sind komplexe mikrobielle Gemeinschaften, die beide Wege, die Ammonifikation oder die Denitrifikation eingehen können.
„Wir ließen der Natur ihren Lauf und konnten in unseren Reaktoren verfolgen, wie die natürliche Selektion die Entscheidung traf, “ sagt Marc Strous, der inzwischen an der Universität von Calgary arbeitet. „So konnten wir die drei kritischen Schalter herausfinden. Die Ergebnisse lassen sich auch auf andere Systeme wie Kläranlagen oder den optimierten Einsatz von Düngemitteln übertragen. Effiziente Düngemittel bedeuten weniger Belastung der Natur.“
Forschungsmeldung der Max-Planck-Gesellschaft vom 8. August 2014.
Beate Kraft, Halina E. Tegetmeyer, Ritin Sharma, Martin G. Klotz,
Timothy G. Ferdelman, Robert L. Hettich, Jeanine S. Geelhoed, Marc Strous
The environmental controls that govern the end product of bacterial nitrate respiration. Science, 8. August 2014, doi: 10.1126/science.1254070

